- Forfatter Jason Gerald gerald@how-what-advice.com.
- Public 2023-12-16 11:30.
- Sist endret 2025-01-23 12:42.
Hvis du synes det periodiske systemet er forvirrende og vanskelig å forstå, ikke bekymre deg, du er ikke alene! Å forstå hvordan det periodiske systemet fungerer kan være vanskelig, men ved å lære å lese det, vil du lykkes i vitenskap. Start med å forstå strukturen på det periodiske bordet og informasjonen den viser om elementene. Deretter kan du studere hvert av elementene. Til slutt, bruk informasjonen som er oppført på det periodiske systemet for å finne ut antall nøytroner i et atom.
Steg
Del 1 av 3: Forstå strukturen i det periodiske systemet
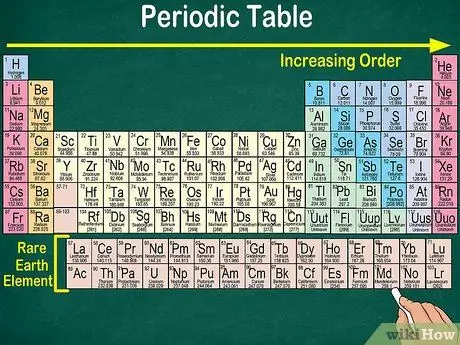
Trinn 1. Les periodisk tabell fra øverst til venstre til nederst til høyre
Elementene er ordnet i henhold til atomnummeret. Jo lenger til høyre og ned, jo høyere atomnummer. Atomnummeret er antall protoner som et element atom har. Når du går lenger til høyre, vil du også legge merke til at massetallet for hvert atom øker. Det vil si at du kan forstå vekten til et element, bare ved å se på plasseringen på bordet.
- Jo lenger til høyre eller ned, vil atommassen til elementet øke fordi atommassen beregnes ved å legge opp protoner og nøytroner i hvert atom av elementet. Antallet protoner øker med elementet, noe som betyr at vekten også øker.
- Elektroner er ikke inkludert i atommassen fordi elektroner ikke har stor effekt på atomvekten sammenlignet med protoner og nøytroner.

Trinn 2. Forstå at hvert element inneholder 1 mer proton enn atomet til venstre
Du kan fortelle dette ved å se på atomnummeret. Atomtallene er ordnet fra venstre til høyre. Elementene er også delt inn i 3 grupper, du kan se grupperingen i tabellen.
For eksempel viser den første raden hydrogen, som har atomnummer 1, og helium, som har atomnummer 2. Disse to elementene er imidlertid plassert helt til venstre og høyre for tabellen fordi de er i forskjellige grupper
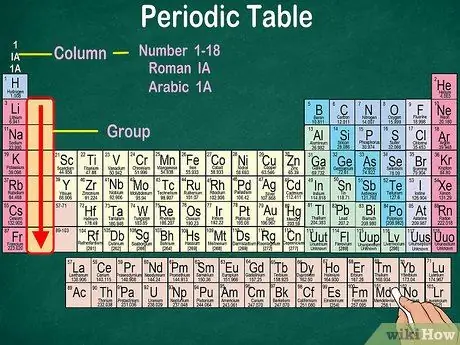
Trinn 3. Identifiser grupper av atomer, som har de samme fysiske og kjemiske egenskapene
Grupper er angitt med vertikale kolonner. I de fleste tilfeller er grupper preget av samme farge. Dette hjelper deg med å identifisere hvilke grunnstoffer som har lignende fysiske og kjemiske egenskaper. Dette vil gjøre det lettere for deg å forutsi reaksjonene til disse elementene. Hvert element i en gitt gruppe har samme antall elektroner i sin ytterste bane.
- De fleste elementene tilhører bare en gruppe. Imidlertid kan hydrogen klassifiseres som enten et halogen eller et alkalimetall. I noen tabeller vises hydrogen i begge gruppene.
- I de fleste tilfeller vil kolonnene bli nummerert 1-18, enten øverst eller nederst i tabellen. Tallene kan vises med romertall (IA), arabiske tall (1A) eller tall (1).
- Les atomgruppene fra topp til bunn.
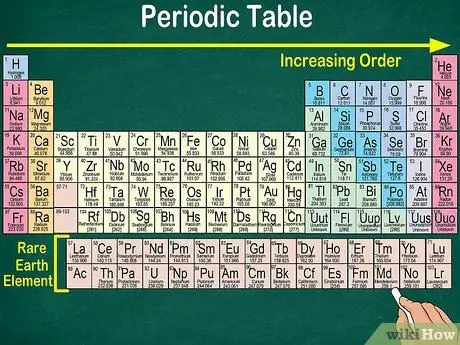
Trinn 4. Legg merke til det tomme rommet i tabellen
I tillegg til atomnummeret, tar arrangementet av elementene i grupper og grupper også hensyn til de samme fysiske og kjemiske egenskapene. På denne måten vil du bedre forstå hvordan hvert element reagerer. Tilsetningen av kjemiske elementer gjør klassifiseringen vanskeligere, så det er ikke overraskende at det periodiske systemet inneholder tomt rom.
- For eksempel har de tre første radene tomme mellomrom, fordi overgangsmetallene som vises i tabellen er elementer som har atomnummer 21.
- På samme måte er elementene 57 til 71, som er sjeldne jordartselementer eller sjeldne jordartselementer, avbildet separat nederst til høyre i tabellen.
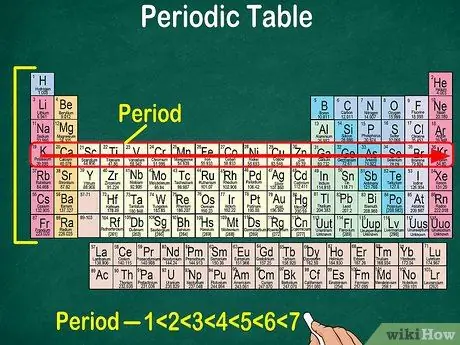
Trinn 5. Legg merke til at hver rad kalles en periode
Alle grunnstoffene i en periode har samme antall atomorbitaler, som elektroner vil passere gjennom. Antall orbitaler vil tilsvare antall perioder. Det periodiske systemet viser 7 rader, noe som betyr at det er 7 perioder.
- For eksempel har et element i periode 1 1 orbital, mens et element i periode 7 har 7 orbitaler.
- I de fleste tilfeller er periodene nummerert 1-7 fra topp til bunn på venstre side av bordet.
- Les perioden for elementene etter raden fra venstre til høyre.
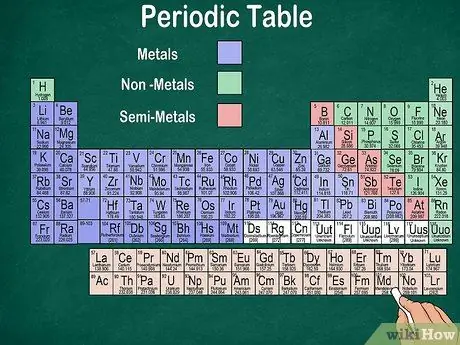
Trinn 6. Skill mellom metaller, halvmetaller og ikke -metaller
Du kan bedre forstå egenskapene til elementer ved å gjenkjenne elementtypen. Heldigvis bruker det meste av det periodiske systemet farge for å indikere om et element er et metall, et halvmetall eller et ikke -metall. Du finner metallelementer til høyre på bordet, mens ikke-metaller til venstre. Halvmetallgruppen ligger mellom metaller og ikke-metaller.
- Husk at hydrogen kan grupperes med halogenene eller alkalimetallene på grunn av dets egenskaper. Derfor er det naturlig at hydrogen vises på begge sider av bordet eller har en annen farge.
- Et element kalles et metall hvis det er skinnende, fast ved romtemperatur, leder varme og elektrisitet, og er mykt og elastisk.
- Et element regnes som et ikke -metall hvis det ikke er skinnende, ikke leder varme eller elektrisitet og er hardt. Disse elementene er vanligvis gassformige ved romtemperatur, men kan også være faste eller flytende ved visse temperaturer.
- Et element kalles et halvmetall hvis det har de kombinerte egenskapene til et metall og et ikke-metall.
Del 2 av 3: Studerer elementene
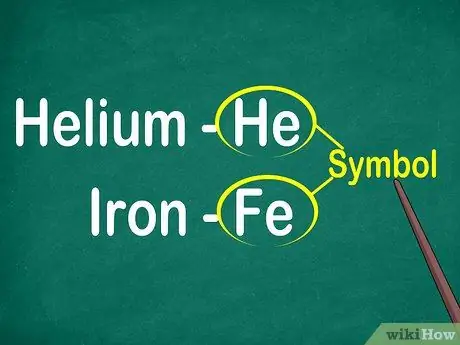
Trinn 1. Identifiser symbolene på 1 til 2 bokstavelementer
Symbolet er vanligvis plassert i midten av et torg med en stor skrift. Symboler er forkortelser for elementnavn, som har blitt standardisert på forskjellige språk. Når du gjør eksperimenter eller arbeider med elementære ligninger, vil du sannsynligvis bruke element symboler. Derfor, om du vil eller ikke, må du gjøre deg kjent med elementære symboler.
Symboler er vanligvis avledet fra det latinske navnet på elementet, men er noen ganger avledet fra navn som er mye brukt, spesielt nye elementer. For eksempel er symbolet for Helium Han, som står for dette velkjente navnet. Imidlertid er symbolet for jern Fe, som er relativt vanskelig å oppdage ved første blikk

Trinn 2. Finn det fulle navnet på elementet, hvis noen
Dette er navnet på elementet du vil bruke hvis du må skrive det ned i sin helhet. For eksempel er "Helium" og "Carbon" navnene på elementer. I de fleste tilfeller er elementnavnet under symbolet, men plasseringen kan variere.
Noen periodiske tabeller inneholder kanskje ikke hele navnet og bruker bare symboler
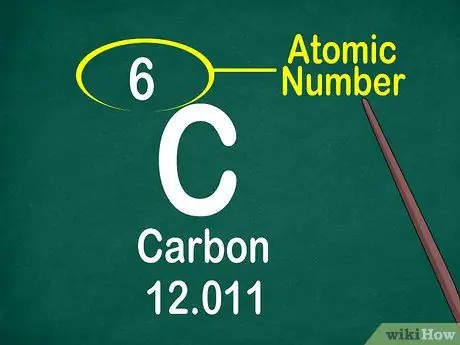
Trinn 3. Legg merke til atomnummeret
Atomnummeret er vanligvis plassert på toppen av boksen, enten i midten eller i hjørnet av boksen. Atomnummeret kan imidlertid også være plassert under elementets symbol eller elementnavn. Atomtallene er ordnet fra 1-118.
Atomnummeret er et heltall, ikke en desimal
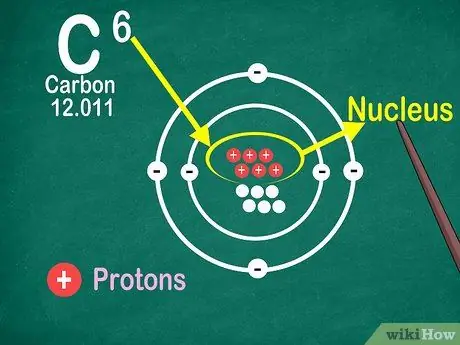
Trinn 4. Vet at atomnummeret er antall protoner i atomet
Alle atomer i et element har samme antall protoner. I motsetning til elektroner kan ikke protoner fanges opp eller frigjøres av atomer. Elementene vil endres hvis atomer kan fange eller miste atomer.
Du trenger også atomnummeret for å finne ut antall elektroner og nøytroner
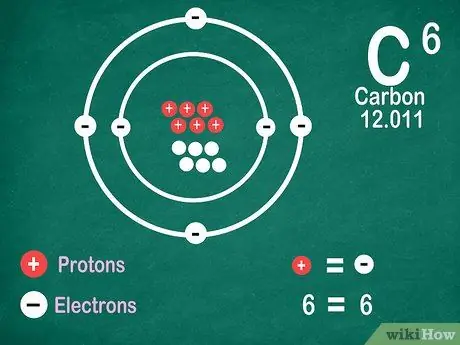
Trinn 5. Vet at elementer inneholder samme antall elektroner som protoner, med mindre elementet gjennomgår ionisering
Protoner har en positiv ladning, mens elektroner har en negativ ladning. Siden et nøytralt atom ikke har elektrisk ladning, betyr det at det har samme antall elektroner og protoner. Atomer kan imidlertid miste og få elektroner, noe som gjør dem ioniserte.
- Ioner er elektriske ladninger. Hvis det er flere protoner i et ion, er ladningen positiv, som er et positivt (+) tegn ved siden av ionesymbolet. Hvis antallet elektroner i ionet er mer, er ladningen negativ, som er negativ (-).
- Du vil ikke se et positivt eller negativt tegn hvis et atom ikke er et ion.
Del 3 av 3: Bruke atomvekt til å telle nøytroner

Trinn 1. Kjenn atomvekten
Atomvekten er vanligvis plassert nederst i esken, under element -symbolet. Atomvekt er den samlede vekten av partiklene i atomkjernen, inkludert protoner og nøytroner. Imidlertid kan ioner komplisere telleprosessen. Atomvekten indikerer således elementets gjennomsnittlige atommasse og atommassen til ionene.
- På grunn av gjennomsnittsvekten har de fleste atomer atomvekter i desimalform.
- Selv om vekten av et element ser ut som om det øker fra venstre til høyre, er det ikke alltid tilfelle.
Trinn 2. Bestem massenummeret til elementet du studerer
Du finner massetallet ved å avrunde atommassen. Dette faktum viser at atomvekten er gjennomsnittet av alle atommasser, inkludert ioner.
For eksempel er atomvekten til karbon 12.011, så det er avrundet til 12. På samme måte er atomvekten til jern 55.847, så det er avrundet til 56
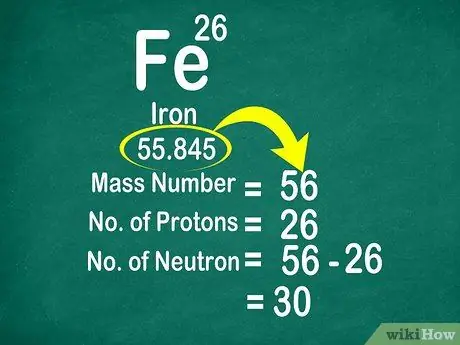
Trinn 3. Trekk massenummeret fra atomnummeret for å telle nøytronene
Massetallet kan beregnes ved å legge antall protoner til antall nøytroner. Dette vil gjøre det lettere for deg å beregne antall nøytroner i et atom, ved å trekke massetallet fra antall protoner
- Bruk denne formelen: Neutron = Massenummer - Proton
- For eksempel er massetallet av karbon 12 og har 6 protoner. Dermed kan vi vite at karbon har 6 nøytroner fordi 12 - 6 = 6.
- Et annet eksempel, massetallet av jern er 56 og har 26 protoner. Dermed vet vi at jern har 30 nøytroner fordi 56 - 26 = 30.
- Isotoper av atomer inneholder forskjellige antall nøytroner, slik at atomvektene endres.
Tips
- Å lese det periodiske systemet er vanskelig for noen mennesker. Ikke bli motløs hvis du synes det er vanskelig å studere det periodiske systemet!
- Fargene i tabellen kan variere, men innholdet forblir det samme.
- Noen periodiske tabeller kan gi ufullstendig informasjon. For eksempel gir noen tabeller bare symbolet og atomnummeret. For det, se etter et bord som passer dine behov!






